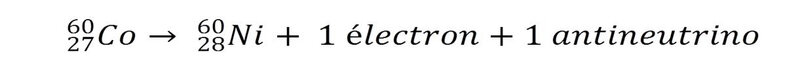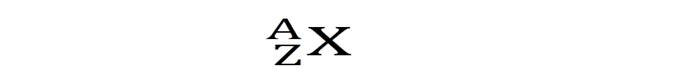La matière est constituée d’atomes. Chacun de ces atomes est lui-même constitué d’un noyau (comprenant des nucléons, c’est-à-dire des neutrons et des protons) et d’électrons qui se trouvent autour du noyau.
Un élément chimique est défini par le nombre de protons de son atome. En effet, le nombre de ses électrons peut varier. Un atome peut « perdre » ou « gagner » des électrons et ainsi devenir un ion. Le nombre de neutrons d’un atome n’est pas non plus fixé à une valeur donnée. Dans la nature, il existe diverses versions du noyau d’un même atome avec des nombres de neutrons différents : ce sont des isotopes. Par exemple, l’uranium 235 et l’uranium 238 sont tous deux des atomes d’uraniums mais le noyau du premier compte 235 nucléons (92 protons et 143 neutrons) et celui du second 238 (92 protons et 146 neutrons) : ce sont deux isotopes de l’uranium.
Dans la nature, certains isotopes sont stables, c’est-à-dire qu’ils n’émettent pas de radioactivité. D’autres, en revanche, présentent un nombre trop important de nucléons (neutrons ou protons) dans leurs noyaux : ils sont qualifiés d’instables et sont radioactifs. Ces noyaux, se désintègrent spontanément pour former des isotopes plus stables, d’un élément qui peut être différent. La radioactivité correspond à ce phénomène où le noyau d’un isotope instable se transforme en un noyau plus stable. Un même élément peut présenter des isotopes stables et des isotopes instables : par exemple le carbone 12 (isotope du carbone dont le noyau comporte 12 nucléons) et le carbone 13 sont stables mais le carbone 14 est instable.
Lors de cette transformation, un rayonnement est également émis. Il existe trois types de rayonnements radioactifs : les rayonnements alpha, beta et gamma.
Le rayonnement alpha, correspond à l’émission de noyaux d’hélium 4 (4He). Lorsqu’un noyau instable se désintègre, il peut se scinder en deux noyaux et ainsi produire un noyau d’hélium et un noyau d’un isotope comportant quatre nucléons de moins que lui et qui est par conséquent plus stable.
Voici un exemple d’une réaction de ce type (N.B. les notations de ces formules sont expliquées à la fin de l’article) :

En d’autres termes, un noyau de radium 226 se désintègre pour produire un noyau de radon 222 et un noyau d’hélium 4 qui correspond au rayonnement alpha. A noter que le radon 222 est lui aussi radioactif. Il va donc à son tour se désintégrer pour produire un noyau comportant moins de nucléons et un noyau d’hélium 4.
Mais tous les isotopes instables ne se transforment pas forcément en émettant un noyau d’hélium. Un autre moyen, pour un atome radioactif, de se rapprocher d’une configuration de noyau stable est le rayonnement beta.
Le cas du rayonnement béta, concerne les noyaux qui contiennent un excès de neutrons. Dans ce cas, les neutrons ont la possibilité de se transformer en proton. Lors de cette réaction, un électron et un antineutrino sont également émis pour conserver le principe de neutralité.
Voici un exemple d’une telle réaction :
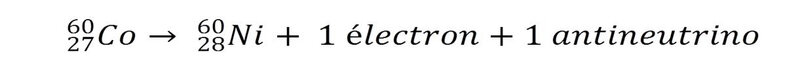
Autrement dit, l’un des neutrons d’un noyau de cobalt 60 (qui comprend 33 neutrons et 27 protons) se transforme en proton. Le nouveau noyau comporte donc maintenant 28 protons. Or, comme nous l’avons vu plus haut, un élément est défini par son nombre de protons. Avec un proton de plus, ce noyau devient donc un noyau de nickel. En l’occurrence, le nickel 60 est un isotope stable du nickel. La réaction s’arrête donc à ce stade.
Le rayonnement gamma, au contraire des deux rayonnements précédents, n’est pas un moyen pour l’atome de retrouver une configuration du noyau plus stable. Ce rayonnement se produit lorsqu’un noyau instable possède une énergie trop grande et permet de décharger cette énergie. Il s’agit d’un rayonnement électromagnétique (tout comme la lumière ou les rayons X, mais d’énergie bien supérieure).
Au final, tout isotope instable a une durée de vie limitée. En se désintégrant, il se transforme en un autre isotope, et ce jusqu’à ce qu’il devienne un noyau stable. La période permet de caractériser la durée de vie d’un isotope radioactif. En effet, elle correspond à la durée au bout de laquelle la quantité de noyaux instables d’un échantillon radioactif sera divisé par deux.
La dangerosité des rayonnements alpha, beta et gamma dépend de l’exposition à ces rayonnements. Les risques dépendent ainsi de trois facteurs :
- La quantité d’atomes radioactifs que contient la source radioactive ;
- La distance d’exposition : plus cette source est proche, plus les risques sont importants ;
- La durée d’exposition : plus le temps d’exposition est grand, plus les risques sont importants.
Néanmoins, de manière générale, le rayonnement gamma est le rayonnement le plus dangereux car c’est le plus pénétrant. En effet, un rayonnement alpha peut être arrêté par une feuille de papier, un rayonnement beta par une feuille d’aluminium, mais un rayonnement gamma n’est pas même arrêté par un mur de béton. Dans les centrales nucléaires, les échantillons émettant des rayonnements gammas sont placés dans des piscines. Une profondeur d’eau suffisante permet effectivement d’absorber les rayons gammas.
Les rayonnements alpha, beta et gamma ne rendent pas la matière qu’ils rencontrent radioactive.
La radioactivité peut être d’origine naturelle ou artificielle. L’écorce terrestre est constituée d’éléments stables et d’éléments radioactifs tels que de l’uranium 238 et le thorium 232 par exemple. Lorsque la Terre s’est formée, elle comportait beaucoup plus d’éléments radioactifs qu’aujourd’hui, mais une grande partie de ceux-ci se sont transformés en éléments stables au fil du temps selon les principes expliqués plus haut. L’uranium 238 et le thorium 232, par exemple ont une période longue (plusieurs milliards d’années) et sont donc encore relativement abondants.
Une autre source de de radioactivité naturelle est la présence de radon dans l’air. Cet élément est un gaz radioactif issu de la transformation radioactive de l’uranium 238 contenu dans l’écorce terrestre. Ce gaz s’échappe donc naturellement dans l’atmosphère.
Le rayonnement cosmique est la troisième source de radioactivité naturelle. Ces rayonnements peuvent transformer certains atomes stables de l’atmosphère en d’autres atomes radioactifs. C’est le cas par exemple du carbone 14. Cet isotope radioactif est créé à partir de l’azote de l’air sous l’action de rayonnements cosmiques.
L’exposition à la radioactivité naturelle n’est pas la même dans tous les endroits du globe, mais demeure généralement faible. En France, chaque personne est exposée en moyenne à 2,4 mSv par an, pour ce qui est de la radioactivité naturelle.
Mais nous sommes également exposés à certaines sources de radioactivité artificielle. Certains radionucléides sont utilisés en médecine, notamment pour des examens et diagnostics. Les doses reçues sont bien entendu minimes et inoffensives.
Les autres sources de radioactivité artificielles concernent les retombées consécutives à des accidents nucléaires et à des essais nucléaires.
Les centrales nucléaires peuvent également rejeter des radionucléides dans leur fonctionnement mais dans des quantités extrêmement infimes. En effet, de très nombreuses précautions sont prises pour confiner les éléments radioactifs dans la centrale.
Au total, en France chaque personne est exposée, en moyenne, à 3,75 mSv par an, dont 2,4 mSv proviennent de la radioactivité naturelle et 1,35 mSv de la radioactivité artificielle. Néanmoins la part relative aux retombées de l’énergie nucléaire et des essais nucléaires ne représentent en moyenne qu’un à deux pourcents de ce chiffre.
Notation des formules :
N.B. : Pour les formules, nous avons utilisé la notation suivante :
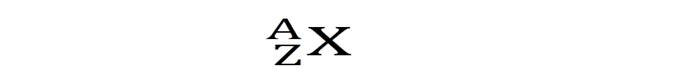
X représente le symbole chimique de l’élément (par exemple U pour uranium, Co pour cobalt, Fe pour fer etc…).
A correspond au nombre de masse. Il s’agit du nombre de nucléons (neutrons plus protons) de l’atome.
Z est le numéro atomique. Il s’agit du nombre de protons de l’atome.